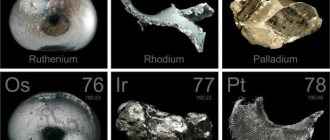
Нахождение в природе
Содержание иридия в земной коре ничтожно мало (10−7 % по массе). Он встречается гораздо реже золота и платины. Встречается вместе с осмием, родием, рением и рутением. Относится к наименее распространённым элементам. Иридий относительно часто встречается в метеоритах. Не исключено, что реальное содержание металла на планете гораздо выше: его высокая плотность и высокое сродство к железу (сидерофильность) могли привести к смещению иридия вглубь Земли, в ядро планеты, в процессе её формирования из протопланетного диска. Небольшое количество иридия было обнаружено в фотосфере Солнца.
Иридий содержится в таких минералах, как невьянскит, сысертскит и ауросмирид.
Добыча иридия
При высокой ценности металла, его количество на нашей планете ничтожно мало. Даже ценная платина не может посоревноваться с его редкостью. В природе в виде самородков чаще всего встречается с примесями других металлов, среди которых рутений, осмий, палладий или платина. В сочетании с этими металлами иридий образует ауросмириды, невьянскиты, осмиридий, сысертскиты. Россыпи иридия можно встретить в местах добычи меди и никеля. Также возможна его добыча из золотых россыпей.
Передовыми странами добытчиками считаются Канада, США, ЮАР, остров Тасмания, Новая Гвинея. Главный поставщик иридия на мировой рынок – ЮАР.
Большую роль в добыче металла играет то, сколько иридия производит ЮАР, а также рост или падение спроса на металл.
Рутений $ 17 за 1 грамм
Металл назван в честь России (от позднелатинского слова Ruthenia — Россия). Это тоже твердый и в то же время весьма хрупкий металл, самый редкий из платиновой группы. Его используют при изготовлении проводов, контактов, электродов, лабораторной посуды, ювелирных изделий. В Западной Европе и Японии все больше металла идет на производство резисторов и печатных схем в электронной промышленности, а также для получения хлора и разных щелочей. Этот металл целиком поступает из ЮАР.
Места добычи
Химический элемент встречается в сплавовом виде в складчатых земных породах гор России, перетонитовых породах, расположенных в ЮАР, Кении, Южной Америке и т. д.
Где есть платина, там есть и иридий.
О характеристиках металла, как химического элемента:
ХарактеристикаОбозначение, значение
| Иридий обозначается символом | Ir |
| Номер в таблице Менделеева | 77 |
| Вес атома | 192,22 а.е.м. |
| Степени окисления | От 1 до 6 (5 не входит) |
| Плотность при комнатной температуре | 22,7 г/см^3 |
| Плотность в жидком состоянии | 19,39 г/см^3 |
| Плавление | При 2300 градусов по Цельсию |
| Кипение жидкого иридия | При 45 градусах Цельсия |
| Имеет кристаллическую решётку | Гранецентрированного куба |
Элемент встречается разных цветов, самый распространённый – белый – KIrF6, лимонный – IrF5, золотой – K3IrCl6, светло-зелёный – Na3IrBr6, розовый – Cs3IrI6, малиновый – Na2IrBr6, тёмно-синий – IrI3. Разнообразие цветов обусловлено наличием в иридии различных солей.
Кстати, название своё металл получил за счёт этого разноцветия. Ирида – это богиня радуги в греческой мифологии.
Получение
Основной источник получения иридия — анодные шламы медно-никелевого производства. Из концентрата металлов платиновой группы отделяют Au, Pd, Pt и др. Остаток, содержащий Ru, Os и Ir, сплавляют с KNO3 и КОН, плав выщелачивают водой, раствор окисляют Сl2, отгоняют OsO4 и RuO4, а осадок, содержащий иридий, сплавляют с Na2O2 и NaOH, плав обрабатывают царской водкой и раствором NH4Cl, осаждая иридий в виде (NH4)2[IrCl6], который затем прокаливают, получая металлический Ir. Перспективен метод извлечения иридия из растворов экстракцией гексахлороиридатов высшими алифатическими аминами. Для отделения иридия от неблагородных металлов перспективно использование ионного обмена. Для извлечения иридия из минералов группы осмистого иридия минералы сплавляют с ВаО2, обрабатывают соляной кислотой и царской водкой, отгоняют OsO4 и осаждают иридий в виде (NH4)2[IrCl6].
Как получают
О том, что этот металл встречается только в сплавах, мы уже сказали. Но каким образом возможно получить иридий? Источником породы является анодный шлам медноникелевого производства. Продукт – шлам насыщают, после чего, под действием «царской водки», переводят из состояния твёрдого в жидкое, в виде соединений хлорида H2[PtCl6].
В результате химики получают жидкую смесь металлов и добавляют в неё хлорид аммония NH4Cl. После чего производят выведение осадка из платины, а потом получают комплекс иридия (NH4)2[IrCl6]. (NH4)2[IrCl6] прокаливают при помощи кислорода и азота. На выходе получаете металлический иридий.
Свойства иридия
Физические свойства иридия достаточно внушительны. Это очень твердый, тяжелый металл, плохо поддающийся механической обработке. Температура плавления составляет 24660С, имеет достаточно высокую температуру кипения 44280С. Его твердость обуславливается плотностью-22,65 г/см3. При нагревании и обычной температуре он устойчив, при температуре до 1000С на все известные кислоты не реагирует. В присутствии хлоридов щелочных металлов при температуре 600-9000С порошок иридия может раствориться хлорированием. Вступает во взаимосвязь с F2, когда температура достигает 4500С. Свойства иридия не играют никакой биологической роли, он не является токсичным металлом, хотя некоторые его соединения очень ядовиты.
Показатели иридия:
- сплавы иридия с вольфрамом и торием используют, как металл для термоэлектрических генераторов; с другими металлами изготавливают топливные баки для космических аппаратов, термопар, термоэмиссионных катодов;
- в автомобильной промышленности применяют в свечах зажигания, что позволяет долго использовать их, хотя они и дорогие;
- находит свое применение в изготовлении перьев для чернильных ручек, на золотых перьях;
- иридий-192 успешно применяют в дефектоскопии, там, где генерирующие источники не могут быть применены, например, во взрывоопасной среде;
- интересно, что из иридия изготовлен эталон килограмма, так как сплав иридия с платиной обладает механической прочностью и не окисляется;
- находит применение в ювелирной промышленности, но цена неимоверно высока на такие украшения;
- изготавливают лабораторные тигли, чтобы проводить опыты с фтором, а также его агрессивными соединениями;
- делают высокопрочные, жаростойкие мундштуки для выдувания стекла.
Материалы и методика под разработку и оптимизацию
Под проведение экспериментов учёными, как правило, берётся чистый иридий, полученный из цилиндрического стержня посредством электроннолучевой зонной плавки. Уровень чистоты иридия составляет 99,95%. Плотность материала отмечается на уровне 22,37 г/см3, тогда как относительная плотность достигает значения 99%, соответственно.
Микро-твёрдость исследуемых структур должна иметь значения не менее 450. Таблица ниже демонстрирует концентрации примесей, характерных для испытательных образцов иридия. Цилиндрические образцы вырезаются из кованого прутка иридия и обрабатываются до конечных размеров 6 и 9 мм по диаметру и длине, соответственно.
| Химический элемент | Количество частей на миллион (ppm) |
| Платина (Pt) | 30 |
| Рутений (Ru) | 30 |
| Родий (Rh) | 10 |
| Палладий (Pd) | 10 |
| Золото (Au) | 10 |
| Серебро (Ag) | 10 |
| Медь (Cu) | 10 |
| Железо (Fe) | 10 |
| Никель (Ni) | 10 |
| Кремний (Si) | 10 |
Методика тестирования горячим сжатием
Достаточно удачной видится методика под эксперименты с применением тестера «Gleeble-1500D». Тестирование деформационного поведения иридия осуществляется здесь при термическом сжатии в диапазоне температур 1200-1500°C и с учётом диапазона скоростей деформации от 10-1 с-1 – 10-3 с-1.
В условиях вакуума образцы предварительно нагреваются до температуры сжатия с учётом скорости нагрева 20°C/с и выдерживаются при этой температуре в течение времени – 60 с. Затем доводятся до истинной деформации — 0,6.
Схема испытаний на горячее сжатие чистого иридия: 1 – температуры деформации; 2 – скорость нагрева; 3 – время выдержки; 4 – скорости деформации; 5 – закаливание водой; T — ось температуры; B — ось времени
Температурное отклонение тестера допустимо в пределах 10°C. Деформированные образцы закаливают, чтобы сохранить деформированную при высокой температуре микроструктуру для последующего анализа. Для исследования профиля твёрдости сжатых образцов применяется вольфрамовый индентор, оснащённый сферическим наконечником.
Для уменьшения трения и повышения равномерности деформации в моменты проведения испытаний на термическое сжатие используют листы графита и тантала. Температурно-временная диаграмма испытания на тепловое сжатие представлена картинкой выше.
Характеристика микроструктуры металла иридий
Образцы для микроструктурного анализа вырезаются из центральной области деформированных образцов по направлению сжатия. Далее образцы шлифуются и вытравливаются электролитической технологией с применением 100 мл насыщенного раствора NaCl, содержащего 35 грамм H и 3–5 грамм HCl.
Аппарат электрической коррозии: 1 – тестовый иридий; 2 – стенка лабораторной колбы; 3 – электролит; 4 – электрод на основе графитового стержня; 5 — амперметр
Аппарат, применяемый для электролитической коррозии, показан на картинке выше. Также используются прецизионные инструменты SEM TM4000PLUS , оптическая микроскопия PMG3 производства «Olympus». Посредством этого набора ведётся наблюдение и анализ деформационной микроструктуры.
При помощи информации: MDPI
Физические свойства
Иридий — тяжёлый серебристо-белый металл, из-за своей твердости плохо поддающийся механической обработке. Температура плавления — 2739 K (2466 °C), кипит при 4701 K (4428 °C). Кристаллическая структура — кубическая гранецентрированная с периодом а0=0,38387 нм; электрическое сопротивление — 5,3⋅10−8Ом·м (при 0 °C), и 2⋅10−7Ом·м (при 2300 °C); коэффициент линейного расширения — 6,5⋅10−6 град; модуль нормальной упругости — 538 ГПа; плотность при 20 °С — 22,65 г/см³, жидкого иридия — 19,39 г/см³ (2466 °С).
Изотопный состав
Природный иридий встречается в виде смеси из двух стабильных изотопов: 191Ir (содержание 37,3 %) и 193Ir (62,7 %). Искусственными методами получены радиоактивные изотопы иридия с массовыми числами 164-199, а также множество ядерных изомеров. Распространение получил искусственный 192Ir.
Химические свойства
Иридий устойчив на воздухе при обычной температуре и нагревании, при прокаливании порошка в токе кислорода при 600—1000 °C образует в незначительном количестве IrO2. Выше 1200 °C частично испаряется в виде IrO3. Компактный иридий при температурах до 100 °C не реагирует со всеми известными кислотами и их смесями. Свежеосажденная иридиевая чернь частично растворяется в царской водке с образованием смеси соединений Ir(III) и Ir(IV). Порошок иридия может быть растворён хлорированием в присутствии хлоридов щелочных металлов при 600—900 °C или спеканием с Na2O2 или BaO2 с последующим растворением в кислотах. Иридий взаимодействует с F2 при 400—450 °C, а c Cl2 и S при температуре красного каления.
Степень окисления иридия
Атомы иридия в соединениях имеют степени окисления 6, 5, 4, 3, 2, 1, 0, -1.
Степень окисления — это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
Ионы иридия
6+Ir 5+Ir 4+Ir 3+Ir 2+Ir 1+Ir
Ir 01-Ir
Валентность Ir
Атомы иридия в соединениях проявляют валентность VI, V, IV, III, II, I.
Валентность иридия характеризует способность атома Ir к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа Ir
Квантовые числа определяются последним электроном в конфигурации, для атома Ir эти числа имеют значение N = 5, L = 2, Ml = -1, Ms = -½
Соединения трёхвалентного иридия
- Ir2O3 — твёрдое тёмно-синее вещество. Малорастворим в воде и этаноле. Растворяется в серной кислоте. Получают при лёгком прокаливании сульфида иридия (III).
- IrCl3 — летучее соединение оливково-зелёного цвета. Плотность — 5,30 г/см³. Малорастворим в воде, щелочах и кислотах. При 765 °C разлагается на IrCl2 и хлор, при 773 °C на IrCl и хлор, а выше 798 °C — на составные элементы. Получают действием хлора на нагретый до 600 °C иридий.
- IrBr3 — оливково-зелёные кристаллы. Растворяется в воде, мало растворим в спирте. Дегидратируется при нагревании до 105—120 °C. При сильном нагревании разлагается на элементы. Получают взаимодействием IrO2 с бромоводородной кислотой.
- Ir2S3 — твёрдое коричневое вещество. Разлагается на элементы при нагревании выше 1050 °C. Мало растворим в воде. Растворяется в азотной кислоте и растворе сульфида калия. Получают действием сероводорода на хлорид иридия (III) или нагреванием порошкообразного металлического иридия с серой при температуре не выше 1050 °C в вакууме.
Соединения четырёхвалентного иридия
- IrO2 — чёрные тетрагональные кристаллы с решёткой типа рутила. Плотность — 3,15 г/см³. Малорастворим в воде, этаноле и кислотах. Восстанавливается до металла водородом. Термически диссоциирует на элементы при нагревании. Получают нагреванием порошкообразного иридия на воздухе или в кислороде при 700 °C, нагреванием IrO2*nН2О.
- IrF4 — жёлтая маслянистая жидкость, разлагающаяся на воздухе и гидролизующаяся водой. tпл 106 °C. Получают нагреванием IrF6 с порошком иридия при 150 °C.
- IrCl4— гигроскопичное коричневое твёрдое вещество. Растворяется в холодной воде и разлагается тёплой (водой). Получают нагреванием (600—700 °C) металлического иридия с хлором при повышенном давлении.
- IrBr4 — расплывающееся на воздухе синее вещество. Растворяется в этаноле; в воде (с разложением), диссоциирует при нагревании на элементы. Получают взаимодействием IrO2 с бромоводородной кислотой при низкой температуре.
- IrS2 — твёрдое коричневое вещество. Малорастворим в воде. Получают пропусканием сероводорода через растворы солей иридия (IV) или нагреванием порошкообразного металлического иридия с серой без доступа воздуха в вакууме.
Соединения шестивалентного иридия
- IrF6 — жёлтые тетрагональные кристаллы. tпл 44 °C, tкип 53 °C, плотность — 6,0 г/см³. Под действием металлического иридия превращается в IrF4, восстанавливается водородом до металлического иридия. Получают нагреванием иридия в атмосфере фтора в трубке из флюорита. Очень сильный окислитель, способный окислить даже воду:
2IrF6 + 10H2O = 2Ir(OH)4 + 12HF + O2, или NO: NO + IrF6 = NO+[IrF6]-
- IrS3 — серый, малорастворимый в воде порошок. Получают нагреванием порошкообразного металлического иридия с избытком серы в вакууме. Строго говоря. не является соединением шестивалетного иридия, так как содержит связь S-S.
- Ir(OH)4 (IrO2*2H2O) образуется при нейтрализации растворов хлороиридатов(IV) в присутствии окислителей. Осадок Ir2O3*nН2О выпадает при нейтрализации щёлочью хлороиридатов (III) и легко окисляется на воздухе до IrO2. Практически нерастворим в воде.
Радуга металла
Открыл металл и дал ему название англичанин С. Теннант, химик. Производя опыты с самородной платиной, химик исследовал и растворы, оставшиеся от опытов. И не зря — в них он обнаружил разноцветные соли неизвестного элемента.
Иридий назвали в честь радуги (по-гречески iris ) — многоцветного чуда.
Это не о цвете металла, это о разнообразии цветов иридиевых солей:
- K3IrCl6, IrF6 — золотисто-желтые кристаллы;
- KIrF6 — белые кристаллы;
- Ir2O3 — синие, сине-черные кристаллы:
- IrCl2 — зеленые кристаллы;
- Na2IrBr6 — малиновый цвет.
Есть соединения иридия, окрашенные в оливковый, коричневый, розовый, золотистый цвета.
Особенности
Сразу стоит сказать, что иридий — это металл. Потому он имеет все те свойства, которые типичны и для иных металлов. Такой химический элемент обозначается сочетанием латинских символов Ir. В таблице Менделеева он занимает 77 клетку. Открытие иридия произошло в 1803 году, в рамках того же исследования, при котором английский ученый Теннант выделил и осмий.
Исходным сырьем для получения таких элементов послужила руда платины, доставленная из Южной Америки. Первоначально металлы выделили в виде осадка, который «не брала» «царская водка». Исследование показало наличие нескольких ранее неизвестных веществ. Свое словесное обозначение элемент получил потому, что его соли выглядят, как будто переливающиеся радугой.
Содержание иридия в природе исключительно мало, и это одно из самых редких веществ на Земле.
Химически чистый иридий не имеет никакого радужного окраса. Зато для него характерен довольно привлекательный серебристо-белый цвет. Токсические свойства не подтверждены. Однако отдельные соединения иридия могут представлять опасность для человека. Особенно ядовит фторид этого элемента.
Производством и аффинажем иридия занимается ряд российских и зарубежных предприятий. Почти весь выпуск этого металла — продукт побочной обработки платинового сырья. Хотя иридий и не пурпурный, он содержит в природном виде 2 изотопа. 191-й и 193-й элементы стабильны. Но выраженные радиоактивные свойства зато имеет ряд искусственно получаемых изотопов, их период полураспада невелик.
[править] Ссылки
- Иридий на Webelements.com.
Электрохимический ряд активности металлов
, , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , , H2
, , , , , , , , , , , , , , ,
Ir, ,
| Периодическая система химических элементов Д. И. Менделеева | |||||||||||||||||||||||||||||||||||||||||||
| Ir | |||||||||||||||||||||||||||||||||||||||||||
| Uue | Ubn | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | ||||||||||||||||||||||||||||||||||||
| Щелочные металлы | Щёлочноземельные металлы | Лантаноиды | Актиноиды | Суперактиноиды | Переходные металлы | Другие металлы | Полуметаллы | Другие неметаллы | Галогены | Благородные газы | Свойства неизвестны | ||||||||||||||||||||||||||||||||
Применение
Особый интерес в качестве источника электроэнергии вызывает его ядерный изомер иридий-192m2 (период полураспада 241 год).
Сплавы с W и Th — материалы термоэлектрических генераторов, с Hf — материалы для топливных баков в космических аппаратах, с Rh, Re, W — материалы для термопар, эксплуатируемых выше 2000 °C, с La и Се — материалы термоэмиссионных катодов.
Иридий используется также для изготовления перьев для ручек. Небольшой шарик из иридия можно встретить на кончиках перьев и чернильных стержней, особенно хорошо его видно на золотых перьях, где он отличается по цвету от самого пера.
Иридий в палеонтологии и геологии является индикатором слоя, который сформировался сразу после падения метеоритов.
Иридий, наряду с медью и платиной, применяется в свечах зажигания двигателей внутреннего сгорания (ДВС) в качестве материала для изготовления электродов, делая такие свечи наиболее долговечными (100—160 тыс. км пробега автомобиля) и снижая требования к напряжению искрообразования. Первой компанией, которая стала использовать иридий, улучшив благодаря этому качество свечей зажигания, стала японская компания NGK. Изначально использовался в авиации и гоночных автомобилях, затем, по мере снижения стоимости продукции, стал употребляться и на массовых автомобилях. В настоящее время такие свечи доступны для большинства двигателей, однако являются наиболее дорогими.
Иридий-192 является радионуклидом с периодом полураспада 74 суток, широко применяемым в дефектоскопии, особенно в условиях, когда генерирующие источники не могут быть использованы (взрывоопасные среды, отсутствие питающего напряжения нужной мощности).
Платиноиридиевый сплав обладает большой механической прочностью, не окисляется. Из этого сплава, в частности, изготовлен эталон килограмма.
В 2013 году иридий впервые в мире был применён в изготовлении официальных монет Национальным банком Руанды, который выпустил монету из чистого металла 999-й пробы. Иридиевая монета была выпущена номиналом 10 руандийских франков.
Промышленность
Свойства металла обусловили сферы применения промышленным комплексом:
- Из иридия делают посуду, оборудование, катализаторы для предприятий химического комплекса.
- В иридиевых тиглях выращивают монокристаллы.
- У автопрома это материал электродов (с медью и платиной) свечей зажигания. Они служат дольше, используются для элитных автомобилей.
- Сплавы иридия с рутением содержат электрогенераторы, термопары для измерения температур до 2000°C.
- Это индикатор качества сварных швов изделий из стали и сплавов алюминия.
Из платиново-иридиевого сплава изготовлены эталоны килограмма и метра (находятся в Париже).
Космические перспективы открыло третье тысячелетие:
- Компания American Elements создала технологию отливки бесшовных иридиевых колец для использования на спутниках, космических аппаратах (2006 год).
- Металл присутствует в дисплеях компьютеров, телевизоров, айфонов, других гаджетов на основе органических светодиодов (технология OLED).
Как источник энергии рассматривается ядерный изомер иридия-192 со временем «жизни» более 240 лет.
Медицина
Из сплава платины с иридием изготовлен хирургический инструментарий, детали кардиостимуляторов.
Это базис для развития ядерной медицины. Радионуклидное сырье получают на ядерных реакторах, циклотронах. 90% уходит на экспорт.
Россия входит в мировую топ-пятерку производителей сырьевых медицинских изотопов.
Иридий-192 задействован при дефектоскопии и онкологами (гамма-нож).
Сказочные перспективы иридия в медицине
В кардиостимуляторах применяется сплав иридий-платина.
Онкологи используют изотоп иридия Ir-192 как источник гамма-излучения. Его применяют для лечения рака груди и предстательной железы (на ранних стадиях болезни).
Разработаны методы лечения эпилепсии, болезни Паркинсона, шизофрении с помощью введения иридиевых электродов в мозг. Радужные перспективы для создания протезов глаза и слухового аппарата открывает метод вживления микроэлектродов.
Ювелирное дело
Ювелиры ценят металл за прочность, используя в сплаве с платиной.
Американская компания Smithson Tennant первой наладила производство ювелирных украшений из иридия. Иридиевые обручальные кольца позиционируются ею как вечные в буквальном смысле: бессильны даже концентрированная кислота и время. Им не требуется особый уход и условия хранения.
Украшения из сплавов с добавлением иридия и через десятилетия выглядят как купленные только что.
Драгоценности с иридием (даже обручальные кольца) не изнашиваются, всегда выглядят как новенькие. Это преимущество особо важно для изделий, испытывающих повышенные нагрузки (обручальные кольца, перстни, браслеты).
Другие сферы
Иридий почитают геологи и палеонтологи: это маркер возраста слоев земной коры и вымерших организмов.
Единственную в мире монету – проба иридия 999 – выпустил в 2013 году Национальный Банк Руанды (государство на востоке Африки). Номинал составил 10 местных франков.
До 1980-х годов шариком из иридиевых сплавов снабжали перья авторучек класса люкс, включая легендарный Parker 51. Это атрибут элиты и аксессуар фаната роскоши Джеймса Бонда.
Калифорний-252 — $ 6 500 000 за 1 грамм
Мировой запас калифорния составляет несколько граммов, вероятно, никак не более 5 г. На Земле только 2 реактора могут нарабатывать его. Один реактор — в России, другой — в США. Каждый из реакторов производит по 20–40 микрограмм в год. Калифорний невероятно дорог. Какие же свойства, несмотря на это, делают этот изотоп столь необходимым?
Калифорний-252 имеет период полураспада 2,6 года. При этом самопроизвольно делится 3% всех атомов и при каждом делении выделяется четыре нейтрона. 1 г в секунду выделяет 2,4 биллиарда нейтронов. Это соответствует нейтронному потоку среднего ядерного реактора! Если бы такое нейтронное излучение захотели получить классическим путем из радиево-бериллиевого источника, то для этого потребовалось бы 200 кг радия. Столь огромного запаса радия вообще не существует на Земле. Даже такое невидимое глазом количество, как 1 мкг калифорния-252, дает более 2 миллионов нейтронов в секунду. Поэтому калифорний-252 в последнее время используют в медицине в качестве точечного источника нейтронов с большой плотностью потока для локальной обработки злокачественных опухолей.
Биологическая роль
Не играет никакой биологической роли. Металлический иридий неядовит, но некоторые соединения иридия, например, его гексафторид (IrF6), очень ядовиты.
Иридий — 77 элемент таблицы Менделеева
Атомная масса элемента №77 равна 192,2. В таблице Менделеева он находится между осмием и платиной. И в природе он встречается главным образом в виде осмистого иридия – частого спутника самородной платины. Самородного иридия в природе нет.
Иридий – серебристо-белый металл, очень твердый, тяжелый и прочный. По данным , это самый тяжелый элемент: его плотность 22,65 г/см3, а плотность его постоянного спутника – осмия, второго по тяжести 22,61 г/см3. Правда, большинство исследователей придерживаются иной точки зрения: они считают, что иридий все-таки немного легче осмия.
Естественное свойство иридия (он же платиноид!) – высокая коррозионная стойкость. На него не действуют кислоты ни при нормальной, ни при повышенной температуре. Даже знаменитой царской водке монолитный иридий «не по зубам». Только расплавленные щелочи и перекись натрия вызывают окисление элемента №77.
Иридий стоек к действию галогенов. Он реагирует с ними с большим трудом и только при повышенной температуре. Хлор образует с иридием четыре хлорида: IrCl, IrCl2, IrCl3 и IrCl4. Треххлористый иридий получается легче всего из порошка иридия, помещенного в струю хлора при 600°C. Единственное галоидное соединение, в котором иридий шестивалентен, – это фторид IrF6. Тонкоизмельченный иридий окисляется при 1000°C и в струе кислорода, причем в зависимости от условий могут получаться несколько соединений разного состава.
Как и все металлы платиновой группы, иридий образует комплексные соли. Среди них есть и соли с комплексными катионами, например [Ir(NН3)6]Cl3 и соли с комплексными анионами, например K3[IrCl3] · 3H2O. Как комплексообразователь иридий похож на своих соседей по таблице Менделеева.
Чистый иридий получают из самородного осмистого иридия и из остатков платиновых руд (после того как из них извлечены платина, осмий, палладий и рутений). О технологии получения иридия распространяться не будем, отослав читателя к статьям «Родий», «Осмий» и «Платина».
Иридий получают в виде порошка, который затем прессуют в полуфабрикаты и сплавляют или же порошок переплавляют в электрических печах в атмосфере аргона. Чистый иридий в горячем состоянии можно ковать, однако при обычной температуре он хрупок и не поддается никакой обработке.
Убить рак: иридий, человеческий сывороточный альбумин и немного синего света
Одним из самых известных супергероев Marvel всегда считался и будет считаться Логан, он же Росомаха. А какая особенность его тела приходит на ум первой, помимо конечно регенерации со скоростью Флеша? Одним словом — адамантий. Этот редкий металл обладает уникальными свойствами, уничтожить его практически невозможно, а переработка занимает уйму сил. У этого выдуманного вещества имеется несколько эквивалентов в нашей с вами реальности, которые также обладают весьма специфическими свойствами. Среди них особое внимание ученых заслужил иридий. Этот металл вряд ли может сделать из простого человека супер-героя, но вот раковые клетки уничтожать он умеет (Дэдпул бы не отказался от такого). Как ученые пришли к такому выводу, насколько эффективен иридий в борьбе с раком и каково его будущее в онкологии? Нырнем в доклад исследовательской группы за ответами. Поехали.
Металловедение
Иридий (Ir) это чрезвычайно твердый переходной металл из платиновой группы. Как и вымышленный адамантий, иридий очень стойко переносит коррозию даже при температуре в 2000 °C. Еще одно сходство этих двух металлов в их внеземном происхождении. Точнее сказать, иридия на нашей планете очень мало, посему в большой концентрации он встречается в местах падения метеоритов.
Иридий (Ir)
Иридий достаточно молодой металл в научном мире, так как был открыт в 1803 году химиком Смитсоном Теннантом. Он воздействовал на платину смесью из азотной и соляной кислот, которая имеет очень необычное название — царская водка. И как понятно из состава этого раствора, после его употребление вы не станете «пьяным мастером», как Джеки Чан в одноименном фильме, а скорее мертвым мастером. Ибо слово «водка» изначально обозначало простую воду и лишь после XIV века начало использоваться для обозначения алкогольного напитка.
С помощью царской водки мистер Теннант смог получить в чистом виде те примеси, которые были в платине, а именно осмий и иридий.
Как уже было сказано ранее, иридия очень мало — в год добывается примерно 3 тонны этого металла. Для сравнения, добыча серебра по некоторым данным превышает отметку в 27000 тонн в год.
Основа исследования
В основе исследования лежит уже применяемый на практике метод лечения онкологических заболеваний (и некоторых других также) — фотодинамическая терапия (ФДТ). Основными героями этого метода являются фотосенсибилизаторы и свет.
Фотосенсибилизаторы*
— вещества, которые увеличивают чувствительность к световому воздействию у биологических тканей.
Сенсибилизаторы достаточно переборчивы, то есть накапливаются только в тех тканях, которые необходимо изменить для дальнейшей процедуры облучения светом.
Когда свет проникает в целевые ткани, происходит фотохимическая реакция — молекулярный триплетный кислород (3O2) преобразуется в синглетный. Помимо этого образуются высокоактивные радикалы. В совокупности это приводит к отмиранию раковых клеток.
Ученые приводят в пример фотофрин и аминолевулиновую кислоту, как самые распространенные фотосенсибилизаторы в ФДТ терапии. Однако в последние годы все больше внимания уделяется металлам с высоким коэффициентом люминесценции, поскольку они обладают необычными и полезными фотохимическими и фотофизическими свойствами. К примеру, TLD1433 (рутений) для ФДТ лечения мочевого пузыря и WST11 (палладий) для лечения сосудов.
Результаты исследования
Так почему не использовать иридий, подумали ученые. Но для начала нужен механизм, который позволит применить этот металл. Не будет же пациент употреблять иридий перорально, как обычные таблетки. И тут к работе подключается человеческий сывороточный альбумин (ЧСА
), который за счет своих свойств и количества (порядка 55% от всех белков крови) является отличным переносчиком различных веществ (в нашем случае лекарственных). Проще говоря, ЧСА можно применить для доставки противораковых препаратов в необходимую область тела пациента, что уже было продемонстрировано в предыдущих исследованиях с применением осмия, рутения и палладия.
Изображение №1
В рассматриваемом нами исследовании ученые создали малеимид-функционализированный октаэдрический органо-иридиевый (III) комплекс Ir1 (1а
) в совокупности с ЧСА. Данный комплекс (Ir1-ЧСА) оказался значительно эффективнее в увеличении фосфоресценции в сравнении с «чистым» Ir1, то есть без ЧСА.
В темноте Ir1-ЧСА по большей степени не токсичен для обычных клеток, но проявляет сильную фото-цитотоксичность по отношению к раковым клеткам и их сфероидам (клеточным образованиям).
Синтезированный Ir1 проявлял стабильность в течение 12 часов в темноте и спустя 1 час облучения синим светом. При этом необходимо было проверить углерод-углеродную связь (С=С). Для этого была проведена реакция комплекса Ir1 и цистеина (Cys) в молярном соотношении Cys: Ir1 — 2:1 в [D6]DMSO/D2O при температуре 298 K в течение 30 минут. В результате протонного магнитного резонанса ученые выяснили пиковый показатель виниловых протонов малеимидных групп на отметке в 6.62 ppm (миллионная доля). При добавлении цистеина пики исчезли, но потом вновь возникли уже в диапазоне 2.9…3.9 ppm. Ученые связывают это с конъюгацией цистеина.
Далее ученые проверили способен ли свободный тиол Cys34 из ЧСА вступать в реакцию с С=С. Для этого 30 μM (микромолль) Ir1 инкубировали с ЧСА (0-120 μM) в течение 1 часа. Далее полученные продукты реакций были разделены с помощью обращённо-фазовой высокоэффективной жидкостной хроматографии (ОФ-ВЭЖХ).
При достижении ЧСА в 120 μM пик Ir1 исчезал полностью (соотношение ЧСА: Ir1 = 4:1). Таким образом содержание тиола (SH) составило 0.27±0.1 моль SH на 1 моль ЧСА (1с
). Следовательно, концентрация свободных SH-групп из 120 μM ЧСА составляет 32.4±1.2 μM. При таком показателе возникает реакция с 30 μM Ir1, приводя к возникновению аддукта (прямого соединения молекул) Ir1 и ЧСА в соотношении 1:1.
Чистый Ir1 не демонстрировал сильного излучения в водном растворе, в отличие от комплекса Ir1-ЧСА (1d
). Чем выше была концентрация ЧСА, тем сильнее становилась фосфоресценция самого Ir1 (
1е
).
Изображение №2
Дабы удалить группы свободных тиолов из ЧСА в раствор было добавлено 100 μM цистина на сутки при температуре 277 K. Полученный продукт соединили с Ir1 на 30 минут. Наблюдения показали значительное снижение фосфоресценции. В случае конъюгата ЧСА-Cys34 и Ir1 (2а
) ситуация была противоположной, а это говорит о том, что именно свободный тиол Cys34 является связующим звеном (правильнее говоря, доменом связывания) для Ir1.
Теперь необходимо было более подробно изучить ЧСА, разобрав его на составляющие. Человеческий сывороточный альбумин имеет одну цепь из 585 аминокислотных остатков, среди которых ученым нужно было найти именно те, что усиливают люминесценцию Ir1. Для этого был проведен люминесцентный анализ взаимодействия Ir1 с различными аминокислотами (2b
и
2с
). И как мы можем видеть на графике
2b
, лидером среди аминокислот с колоссальным отрывом стал гистидин (His), усиливающий люминесценцию Ir1 в 37 раз.
Немного разобравшись в том, что и как работает внутри составных компонентов комплекса Ir1-ЧСА, ученые перешли к практическому применению, то есть к опытам.
Сначала 0.4 миллимоль Ir1 разбавили в 20 мл MeOH:H2O, добавили 0.4 миллимоль HSA и перемешивали в течение 1 часа. Далее с помощью конфокальной микроскопии было исследовано распространение Ir1-ЧСА в живых клетках рака легких (A549).
Уже спустя 30 минут Ir1-ЧСА по большей степени концентрировался в цитоплазме раковых клеток. На 60-120 минуте от начала инкубации, комплекс проникал в ядра клеток рака.
Изображение №3: конфокальная микроскопия клеток рака легких A549.
Однако стоит отметить, что не весь комплекс проникал в ядра раковых клеток, а только Ir1. Проверка иммунофлуоресцентным методом показала, что ЧСА просто отсутствует в ядрах клеток, попавших под воздействие Ir1.
Изображение №4: иммунофлуоресцентный анализ наличия ЧСА в клетках рака легких.
Но ЧСА не исчезает бесследно, он просто остается в цитоплазме и в мембране ядра клетки рака. Получается, что ЧСА полностью выполняет свою функцию: он доставил Ir до ядра клетки, а сам остался снаружи.
Изображение №5: квантовый выход и время жизни фосфоресценции Ir1 и комплекса Ir1-ЧСА.
Ученые также проверили квантовый выход (утрировано, силу) и время жизни фосфоресценции Ir1 (самого по себе) и комплекса Ir1-ЧСА.
Квантовый выход Ir1 был очень мал (всего лишь 0.001), а время жизни при температуре 298 K составило 182.7 наносекунд (5а
). А вот у Ir1-ЧСА квантовый выход был уже 0.036, а время жизни — 871.8 нс. Такая продолжительность фосфоресценции отлично способствует генерации синглетного кислорода (1 O2).
Спектроскопия электронного парамагнитного резонанса с использованием 2,2,6,6-тетраметилпиперидина в качестве спиновой ловушки помогла обнаружить генерацию 1O2 в чистом Ir1 и в комплексе Ir1-ЧСА при иррадиации в 465 нм в течение 20 минут (5b
). Как и ожидалось, квантовый выход 1O2 у Ir1-ЧСА был значительно выше (0.83), чем у Ir1 (0.06).
Также необходимо было проверить степень воздействия Ir1-ЧСА и Ir1 на раковые клетки и на здоровые. В качестве раковых клеток выступило три варианта: рак легких A549, гепатома Hep-G2 и устойчивый к цисплатину рак легких A549R. В качестве здоровых клеток использовались MRC-5 (легкие) и LO2 (печень). Эксперимент проводился в двух вариациях освещения: полная темнота на протяжении всего опыта и синий свет.
Клетки инкубировали Ir1 или Ir1-ЧСА в течение 2 часов, промывали с помощью пербората натрия и облучались синим светом в течение 20 минут либо оставляли в темноте (второй вариант опыта). После этого клетки восстанавливались в течение 46 часов.
Воздействие Ir1 на клетки A549 и в темноте (89.6 μM), и при освещении (53.3 μM) практически отсутствовало.
Таблица воздействия Ir1 и Ir1-ЧСА на раковые клетки: чем больше число, тем меньше воздействия (т.е. больше клеток рака остались невредимы).
А вот Ir1-ЧСА показал совсем иные результаты. В темноте испытуемый комплекс никак не влиял на раковые клетки, но при освещении степень его цитотоксичности значительно возросла. Подобные результаты, как мы с вами видим из таблицы выше, Ir1 и Ir1-ЧСА показали и по отношению к другим раковым клеткам. При этом здоровые клетки и в темноте, и при освещении не были затронуты Ir1 и Ir1-ЧСА.
Напоследок ученые провели анализ активных форм кислорода (АФК) внутри клеток после светового облучения. В темноте, как и ожидалось, никаких АФК обнаружено не было. А вот в клетках, которые подвергались световому облучению после применения Ir1-ЧСА, АФК были обнаружены (5с
).
Для более детального ознакомления с исследованием настоятельно рекомендую заглянуть в доклад ученых и дополнительные материалы к нему.
Эпилог
Данным исследованием ученые не пытались изобрести велосипед в виде применения редких металлов в фотодинамической терапии, ибо это уже было сделано ранее с осмием и палладием. Однако никто еще не пробовал использовать иридий, что исследователи и решили исправить. Их труд не оказался бесполезен, так как иридий показал отличные результаты в борьбе с раковыми клетками разных типов, при этом не затрагивая здоровые.
Онкологические заболевания — одни из самых распространенных, каждый год забирающих миллионы жизней. Изобретение новых методов борьбы с этим недугом и совершенствование имеющихся должно и будет продолжаться. Конечно, нам пока еще далеко до тотальной победы над раком, но ученые по всему миру продолжают свою борьбу в лабораториях, как и миллионы больных в палатах.
Не стоит также забывать и факторах, которые приводят к возникновению онкологических заболеваний. Часть из них (экология, вредные привычки и т.д.) человеку вполне по силам ликвидировать.
Пятничный оффтоп:Никто в здравом уме не обрадуется онкологии. Подобные диагнозы заставляют опустить руки и забыть обо всем. Но сдаваться никогда нельзя. Если не бороться, диагноз однозначно возьмет верх. А если же бороться с болезнью, всегда есть шанс на победу над ней. Так почему бы этот шанс не использовать?
Благодарю за внимание, оставайтесь любопытствующими и отличных всем выходных, ребята.
Спасибо, что остаётесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас оформив заказ или порекомендовав знакомым, 30% скидка для пользователей Хабра на уникальный аналог entry-level серверов, который был придуман нами для Вас:
Вся правда о VPS (KVM) E5-2650 v4 (6 Cores) 10GB DDR4 240GB SSD 1Gbps от $20 или как правильно делить сервер? (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
VPS (KVM) E5-2650 v4 (6 Cores) 10GB DDR4 240GB SSD 1Gbps до весны бесплатно
при оплате на срок от полугода, заказать можно тут.
Dell R730xd в 2 раза дешевле?
Только у нас
2 х Intel Dodeca-Core Xeon E5-2650v4 128GB DDR4 6x480GB SSD 1Gbps 100 ТВ от $249 в Нидерландах и США!
Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?
Искусственный иридий
Иридий, как и многие другие металлы крайне редкий, но очень ценный и широко используемый металл. Спрос на такие металлы только нарастает, а их количество природе уменьшается и к большому сожалению человечества не возобновляется. В связи с этим в мире большие обороты набирает искусственный синтез драгоценных металлов. Для этого создаются целые компании и лаборатории. Самой передовой и успешной технологией искусственного синтеза драгметаллов, которую только начинают внедрять является холодная ядерная трансмутация. Этот способ признан в мире и сегодня с его помощью синтезируется искусственная платина. Над остальными металлами проводятся работы. На территории России искусственным синтезом занимается .
Золото $ 45 за 1 грамм
Золото — главный драгоценный металл, признанный таковым по всему миру с древнейших времён. Золото словно самой природой создано для чеканки монет и производства ювелирных украшений: оно встречается исключительно в чистом виде, пластично и устойчиво к коррозии, однородно, компактно, короче, — идеальный, в некотором смысле, металл. Сейчас можно золото купить и в ювелирных магазинах, и в банках.
Интересные факты
Соли иридия очень разнообразны по окраске. Так, в зависимости от числа присоединившихся атомов хлора, соединение может иметь медно-красный, темный зеленый, оливковый или коричневый цвета. Дифторид иридия окрашен в желтый тон. Соединения с озоном и бромом имеют синюю окраску. У чистого иридия коррозионная стойкость очень велика даже при нагреве до 2000 градусов.
В породах земного происхождения концентрация иридиевых соединений очень невелика. Серьезно повышается она только в породах метеоритного происхождения. Такой критерий позволяет исследователям установить важные факты о различных геологических структурах. Всего на земле производится лишь несколько тонн иридия.
Модуль Юнга (он же модуль продольной упругости) у этого металла — на втором месте среди известных веществ (больше — только у графена).
Источники
- https://chem.ru/iridij.html
- https://mysamocvet.ru/metally/iridij/
- https://ProDragmetally.ru/dragotsennye-metally/iridij.html
- https://himsnab-spb.ru/article/ps/ir/
- https://metallsmaster.ru/iridij/
- https://k-tree.ru/tools/chemistry/periodic.php?element=Ir
- https://TheMineral.ru/metally/iridij
- https://vplate.ru/metally-i-splavy/vse-ob-iridii/
- https://jgems.ru/metally/iridij
- https://calcsbox.com/post/iridium.html